Redwood: 品質検査結果のレポート時に電子レコードおよび電子シグネチャを使用
U.S. Food and Drug Administration's (FDA)が管理するクリティカル・トランザクションGood Manufacturing Practices (GMP)の要件には、電子シグネチャ(電子シグネチャ)および電子記録(電子記録)の使用を必要とする組込みの検証が含まれます。
この更新では、Redwoodユーザー・エクスペリエンスを介して検査結果をレポートする際に、電子シグネチャ承認を取得し、対応する電子レコードを表示できます。
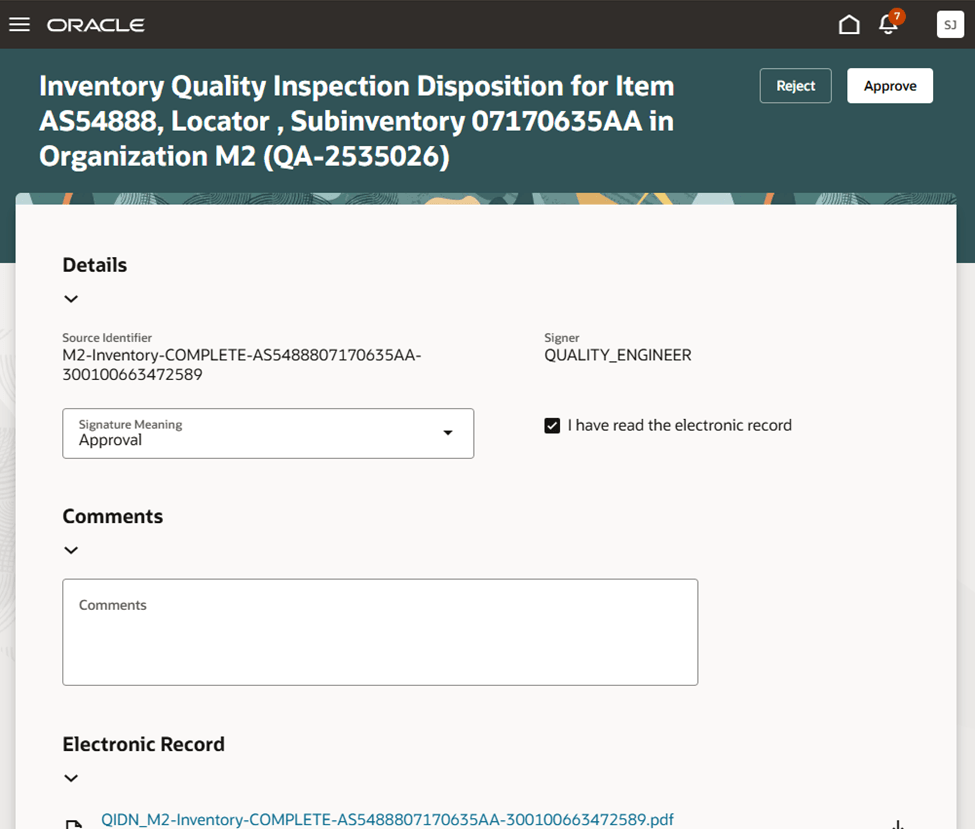
Redwood書式での承認発行
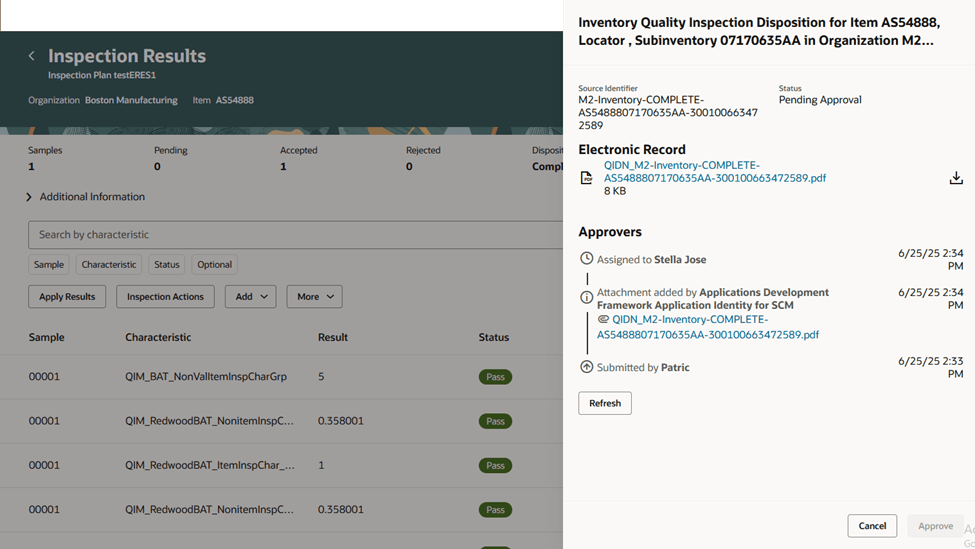
Redwood書式での電子シグネチャ承認
- 安全な電子シグネチャおよび電子記録管理を通じて、FDA 21 CFR Part 11規制への準拠を保証
- 手作業によるエラーのリスクを軽減し、検査レポートにおけるデータの整合性を改善
- デジタル・サインオフ・ワークフローを可能にすることで、承認プロセスを迅速化
これらの機能のデモを次に示します:
有効化のステップ
- 「サプライ・チェーン管理トランザクションの電子レコードおよび電子署名の取得」機能のオプトインを有効にします。
- タスク「電子シグネチャ・プリファレンスの構成」で組織の品質検査処分インライン電子シグネチャ承認を使用可能にして、電子シグネチャ・プリファレンスを構成します。 「電子署名プリファレンスの構成」を参照してください。
- トランザクションの電子署名を有効にした後、「サプライ・チェーン管理のタスク構成の管理」タスクを使用して、構成可能なビジネス・プロセス・ルールをOracle Business Process Managementで定義し、「設定および保守」作業領域の「承認グループの管理」タスクで各トランザクションの承認者も決定してください。
ヒントと考慮事項
- 電子署名承認は、ユーザー・インタフェースを介してのみサポートされます。 RESTリソースを使用して電子シグネチャ承認を指定することはできません。
主なリソース
アクセス要件
次の権限およびコードを含む構成済ジョブ・ロールが割り当てられているユーザーは、この機能にアクセスできます:
品質検査管理権限 :
- 検査結果の編集(QA_EDIT_INSPECTION_RESULTS)
電子署名承認権限:
- 電子署名(EDR_ADD_ESIGNATURES_TRANSACTIONS_PRIV)
- 電子レコードおよび署名の表示(EDR_VIEW_RECORDS_ESIGNATURES_PRIV)